采用Fenton法预处理垃圾渗滤液,考察了初始pH值、FeSO4•7H2O投加量、H2O2/Fe2+物质的量比及反应时间对Fenton氧化处理效果的影响。研究的主要结论如下:(1)pH、n(H2O2)/n(Fe2+)、FeSO4•7H2O投加量是影响Fenton氧化处理效果的主要因素,反应时间对其也有一定影响。
这些因素的主次关系为:(1)pH>n(H2O2)/n(Fe2+)>FeSO4•7H2O投加量>反应时间;(2)在pH为3.0、FeSO4•7H2O投加量为1.2mmol/L、H2O2与Fe2+摩尔比为8:1、反应时间为30分钟条件下,COD去除率可达到62.3%。
生活垃圾经环卫系统收集压缩以后运输至垃圾焚烧发电厂垃圾库,垃圾经堆放、压缩、发酵以后产生渗滤液,垃圾渗滤液属原生垃圾渗滤液,我国大部分城市生活垃圾的厨余物多,含水率高、热值低,炉排炉直接焚烧处理垃圾时必须将新鲜垃圾在垃圾库中储存5~7天进行发酵,以达到滤出水份、提高热值,保证后续垃圾焚烧的正常运行和炉膛温度。
垃圾渗滤液会对周围的环境造成严重的影响,如何有效处理垃圾渗滤液成为近年来的研究热点[1-11]。本研究采用Fenton法预处理垃圾渗滤液,对其预处理效果进行研究,为Fenton法应用于垃圾渗滤液预处理提供一些参考。
1 材料及方法
1.1 实验材料与仪器
实验试剂:浓硫酸、氢氧化钠、硫酸亚铁铵、七水合硫酸亚铁、重铬酸钾、硫酸-硫酸银、一水合邻菲咯啉、双氧水、硫酸汞。
实验废水:实验所用的垃圾渗滤液取自泰州市某垃圾焚烧发电厂,通过初步测定,废水的pH值在6.53左右,COD为10200mg/L。颜色呈现黑褐色,并伴有恶臭味。
实验仪器:电子天平、pH计、COD消解器。
1.2 实验方法
取一定量的垃圾渗滤液于500ml的烧杯中,调节pH值,再加入一定量的FeSO4•7H2O和双氧水,搅拌反应一段的时间后,静置30分钟,然后取其上清液测定COD。分别改变反应条件中的初始pH值、FeSO4•7H2O投加量、H2O2/Fe2+物质的量比及反应时间,考察这些条件对处理效果的影响。
2 结果与讨论
2.1 初始pH值的影响
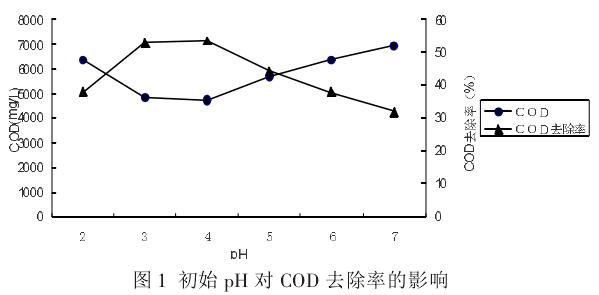
取6份100ml的垃圾渗滤液,加入到6个500ml的烧杯中,分别调节pH值到2.0、3.0、4.0、5.0、6.0、7.0,再加入5.0ml/L的双氧水和5mmol/L的FeSO4•7H2O,搅拌反应时间设定为1个小时。反应完成后静置30分钟后取其上清液测定COD,实验结果如图1所示。
由图可知,当pH在2~4范围之内,随着pH的增加COD的去除率呈现了上升的趋势,并在pH=4.0时COD去除率为最大。当pH大于4时,随着pH值的增加,COD去除率则逐渐呈下降的趋势。
这是由于在酸性条件下对H2O2的分解和•OH产生比较有利,并且Fe2+的催化效率比较高,但随着pH的升高,会有一部分Fe2+被氧化为Fe3+,而Fe3+的催化效果则不如Fe2+,也降低了•OH的氧化活性,所以对COD的去除效果会下降。由于在pH为3和4时的去除率比较相近,出于对经济性的考虑,最佳pH值为4.0。
2.2 Fe2+投加量的影响
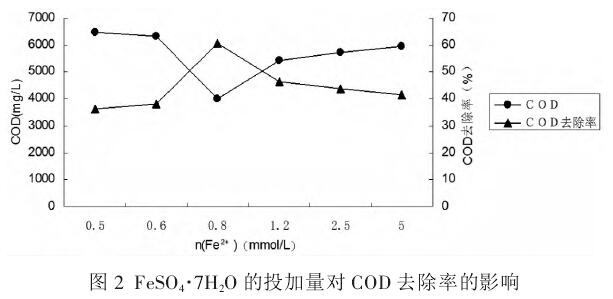
分别取100ml的垃圾渗滤液,加入6个到500ml的烧杯中,调节pH值到4.0,固定双氧水投加量为5.0ml/L,FeSO4•7H2O的投加量分别为5、2.5、1.2、0.8、0.6、0.5mmol/L,搅拌反应时间设定为1个小时。反应完成后,静置30分钟后取其上清液测定COD,实验结果如图2所示。
由图可以看出,当Fe2+浓度在0.5~0.8mmol/L的范围内时,随着FeSO4•7H2O投加量的逐渐增加,COD去出率明显地呈现上升趋势,在0.8mmol/L时COD去除率达到最大,但继续增加投加量时,去除率反而开始缓慢地降低。
这是因为随着Fe2+的增加,催化H2O2产生的•OH也会随之增加,但是当Fe2+投加过量时,多余的Fe2+则会与•OH反应产生Fe3+,并且会消耗掉一部分的双氧水,使其活性降低,影响了COD的去除。因此最佳的FeSO4•7H2O投加量为0.8mmol/L。
2.3 H2O2与Fe2+物质的量比的影响
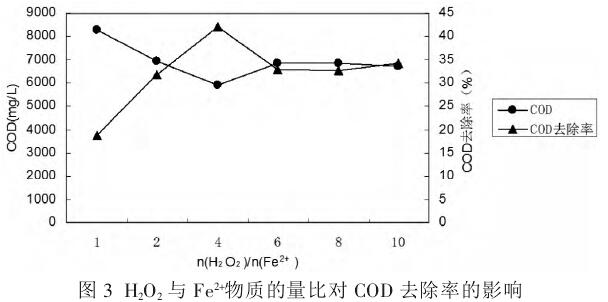
分别取100ml的垃圾渗滤液到6個500ml的烧杯中,调节pH值到4.0,固定FeSO4•7H2O的投加量为0.8mmol/L,调节H2O2与Fe2+摩尔比1:1、2:1、4:1、6:1、8:1、10:1,搅拌反应时间设定为1个小时。反应完成后静置30分钟,取其上清液测定COD,实验结果如图3所示。
由图可知,H2O2与Fe2+摩尔比对COD去除率的影响比较明显,当H2O2与Fe2+摩尔比在1~4之间时,随着H2O2与Fe2+摩尔比的增大,COD去除率上升得比较快,并在4:1的时候COD去除率达到了最大值,之后则呈现了下降趋势,并且有较小的波动。
这是由于随着n(H2O2)/n(Fe2+)的增加,产生的H2O2量较多,则生成•OH的量也会增多,氧化能力就得到了提升。但当H2O2过量时,溶液中的一部分Fe2+会被氧化成Fe3+,而且Fe3+会抑制•OH的产生,并且其中一部分自由基也会与•OH产生反应,这些都造成了•OH的减少则减弱了氧化能力。因此,最佳的H2O2与Fe2+摩尔比为4:1。
2.4 反应时间的影响
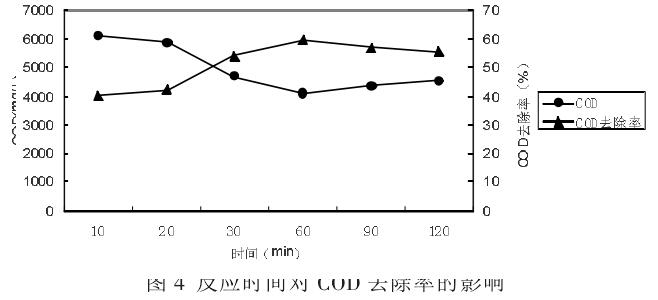
分别取100ml的垃圾渗滤液加入到6个500ml的烧杯中,调节pH 到4.0,固定FeSO4•7H2O的投加量为0.8mmol/L,H2O2与Fe2+摩尔比为4:1,控制反应时间为10、20、30、60、90、120min,反应完成后静置30分钟,取其上清液测定COD,实验结果如图4所示。
由图可知,反应时间在60min之前,随着时间的增加,COD去除率在逐渐地上升,并在60min时COD去除率到达最大,之后呈缓慢的下降趋势。这是由于在短时间内,随着反应时间增加,反应越充分,产生的•OH也会变多,但是到达一定时间后,反应中的过氧化氢和亚铁离子浓度降低,则产生的•OH的量就会减少,导致氧化能力下降,去除率就会有所下降。因此确定Fenton法去除COD的最佳反应时间为1个小时。
2.5 正交实验及结果
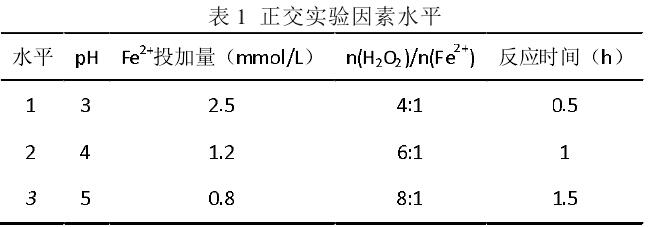
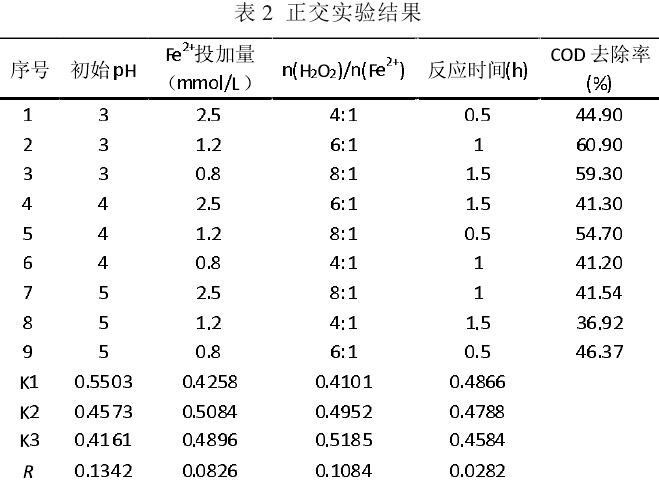
根据单因素的实验结果,选取初始pH、FeSO4•7H2O投加量、H2O2与Fe2+摩尔比、反应时间进行4因素3水平的正交实验。正交实验因素及其水平见表1,实验结果如表2所示。
从正交实验的结果可以看出,最佳的反应条件为:初始pH为3.0,FeSO4•7H2O投加量为1.2mmol/L,H2O2与Fe2+摩尔比为8:1,反应时间为30分钟。在此条件下COD的去除率达到了62.30%。通过对极差的结果分析可知这些因素中初始pH的影响尤为重要,其次是 H2O2与Fe2+摩尔比,然后再是FeSO4•7H2O投加量,反应时间的影响比较小。
3 结论
采用Fenton法预处理垃圾渗滤液,研究初始pH、FeSO4•7H2O投加量、H2O2与Fe2+摩尔比、反应时间对垃圾渗滤液处理效果的影响,得出结论如下:(1)初始pH、FeSO4•7H2O投加量、H2O2与Fe2+摩尔比、反应时间都对COD去除率有一定的影响,其中影响最大的是初始pH值,其次是H2O2与Fe2+摩尔比,然后再是FeSO4•7H2O投加量,最后是反应时间。(2)由正交实验得出最佳的实验条件为初始pH为3.0、FeSO4•7H2O投加量为1.2mmol/L、H2O2与Fe2+摩尔比为8:1、反应时间为30分钟,在此条件下的COD去除率为62.3%。